مقدمة: ما وراء المكونات التقليدية للقاحات
على مدار العقد الماضي، توصل العلماء في جامعة «نورث وسترن» إلى بصيرة جوهرية حول آليات عمل اللقاحات؛ فبينما تُعد المكونات الكيميائية حاسمة، إلا أن الطريقة التي يتم بها تنظيم تلك المكونات ماديًا وتوزيعها في الفراغ يمكن أن تؤثر بشكل درامي على الأداء المناعي. هذا المفهوم وضع حجر الأساس لما يعرف اليوم بـ «الطب النانوي الإنشائي» (Structural Nanomedicine)، وهو مجال ناشئ يركز على تصميم الأدوية من «الأسفل إلى الأعلى» لضمان أقصى قدر من الفعالية وأقل قدر من السمية.
في دراسة حديثة نُشرت في دورية Science Advances، طبق الباحثون هذا المفهوم على اللقاحات العلاجية الموجهة للأورام الناتجة عن فيروس الورم الحليمي البشري (HPV). واكتشف الفريق أن مجرد تعديل موضع واتجاه ببتيد واحد يستهدف السرطان أدى إلى تعزيز قدرة الجهاز المناعي بشكل كبير على مطاردة الخلايا الورمية وتدميرها.
المنهجية: لغز الأحماض النووية الكروية
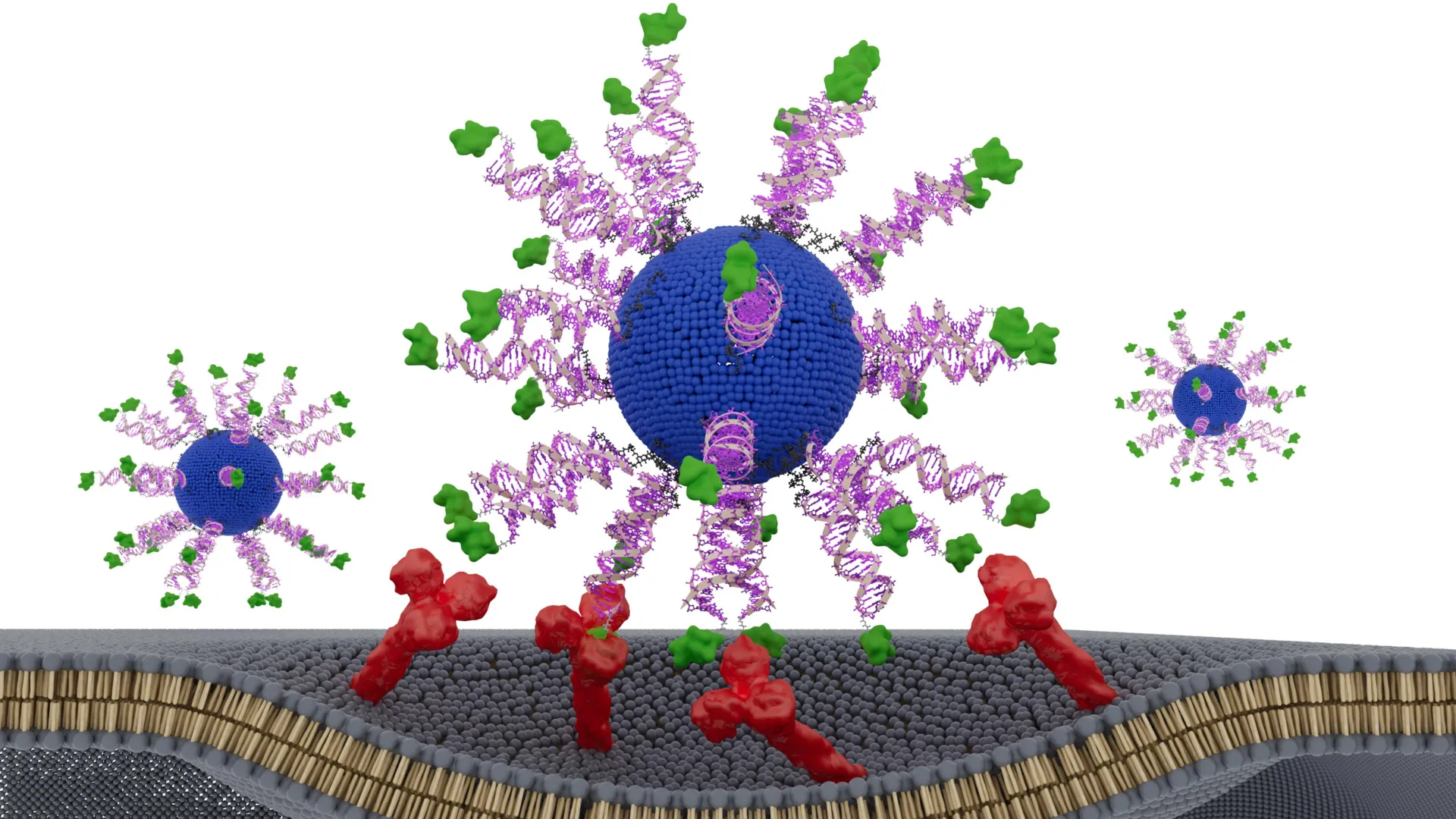
لاستكشاف هذه الفرضية، صمم الفريق بقيادة البروفيسور «تشاد ميركين»، رائد تقنية النانو، لقاحًا يعتمد على «الأحماض النووية الكروية» (SNAs). وهي هياكل كروية من الحمض النووي (DNA) تمتلك قدرة طبيعية على اختراق الخلايا المناعية وتنشيطها. قام الباحثون بإعادة تنظيم مكونات اللقاح داخل هذه الهياكل في عدة تكوينات مختلفة، مع تثبيت المكونات نفسها في كل نسخة.
تم اختبار هذه التكوينات في نماذج حيوانية «مُؤنسنة» (تتمتع بجهاز مناعي بشري) مصابة بسرطان إيجابي لفيروس HPV، وكذلك في عينات أورام حقيقية مأخوذة من مرضى يعانون من سرطان الرأس والرقبة. ركزت الدراسة على مقارنة ثلاثة تصميمات أساسية: في التصميم الأول، تم إخفاء «الببتيد» المستهدف داخل الجسيم النانوي، بينما تم عرضه على السطح في التصميمين الآخرين، مع تغيير طرف الارتباط (النهاية النيتروجينية N-terminus مقابل النهاية الكربونية C-terminus).
الاكتشاف: الهندسة الجزيئية تحدد مصير الورم
أظهرت النتائج أن أحد التكوينات تفوق بوضوح على البقية؛ حيث أدى عرض المستضد (Antigen) على السطح وربطه عبر نهايته النيتروجينية إلى توليد استجابة مناعية أقوى بثماني مرات من حيث إنتاج «إنترفيرون غاما»، وهو جزيء إشارة حيوي تطلقه الخلايا التائية القاتلة لتدمير الخلايا السرطانية.
هذا الترتيب الهندسي الدقيق لم يقلل من نمو الورم فحسب، بل أدى أيضًا إلى إطالة عمر الحيوانات الخاضعة للتجربة، وزيادة أعداد الخلايا التائية من نوع (CD8) عالية النشاط. ويوضح هذا الاكتشاف أن «نهج الخلاط» التقليدي — حيث يتم خلط المكونات معًا دون تحكم هيكلي — قد يفوت فرصًا هائلة لتحقيق استجابات مناعية قوية. الجهاز المناعي، كما اتضح، حساس للغاية لهندسة الجزيئات وكيفية معالجتها داخل الخلية.
الأهمية العلمية والسريرية
تكمن أهمية هذه الدراسة في تحول النموذج من البحث عن «مكونات سحرية» جديدة إلى «تحسين هيكلي» للمكونات المتاحة بالفعل. تسبب فيروسات HPV معظم حالات سرطان عنق الرحم ونسبة متزايدة من سرطانات الرأس والرقبة. وبينما تمنع اللقاحات الوقائية الإصابة بالعدوى، إلا أنها لا تعالج السرطانات القائمة. وهنا تأتي أهمية هذه اللقاحات العلاجية التي تدرب الخلايا التائية على «اصطياد» الخلايا المصابة.
يشير البروفيسور ميركين إلى أن هذا النهج قد يُنقذ العديد من اللقاحات المرشحة التي فشلت سابقًا في التجارب السريرية؛ فربما لم تكن المكونات هي المشكلة، بل الطريقة التي قُدمت بها للجهاز المناعي. ومن خلال تحسين الهيكل النانوي، يمكننا بناء أدوية أكثر قوة بأقل جرعات ممكنة، مما يقلل من الآثار الجانبية.
الآفاق المستقبلية: الذكاء الاصطناعي والطب الشخصي
يتطلع الفريق الآن إلى دمج الذكاء الاصطناعي في تصميم اللقاحات، حيث يمكن لأنظمة التعلم الآلي تحليل آلاف التكوينات الهيكلية المحتملة لتحديد الترتيبات الأكثر فعالية بسرعة فائقة. إن استراتيجية الطب النانوي الإنشائي لا تقتصر على فيروس HPV فحسب، بل يتم اختبارها بالفعل لاستهداف أنواع أخرى من السرطانات مثل الميلانوما وسرطان الثدي ثلاثي السلبية وسرطان البروستاتا.
إن الانتقال من التوليف الكيميائي العشوائي إلى الهندسة النانوية الدقيقة يمثل حقبة جديدة في الطب؛ حقبة لا نهتم فيها فقط بما تحتويه الزجاجة، بل بكيفية اصطفاف كل ذرة وجزيء لضمان انتصار الجهاز المناعي في معركته ضد السرطان.
المصدر العلمي: ScienceDaily

اترك تعليقاً